台灣國產的高端疫苗,在國內已經開放接種超過2個月,第一劑接種人次超過75萬人,不過高端疫苗一上路就倍受爭議,從臨床試驗數據到沒有國際認證,都是外界提出質疑的地方,不過世界衛生組織WHO在10月26日宣布,啟動「團體試驗疫苗」(Solidarity Trial Vaccines)計畫,台灣國產高端疫苗被列為候選疫苗,預計將與南美洲國家哥倫比亞、西非國家馬利和菲律賓共同合作。
WHO表示,「團體試驗疫苗」是一個跨國、隨機臨床試驗平台,目的在快速評估前景可期的新候選疫苗的防護力和安全性,除了高端的次單位重組蛋白疫苗,另一則是美國伊諾維奧製藥公司(Inovio)的脫氧核糖核酸(DNA)疫苗,從20款COVID-19疫苗中選出兩款。
中央流行疫情指揮中心指揮官陳時中表示,WHO贊助高端疫苗有三大意義,第一個意義是在各國研發的COVID-19疫苗中,意味高端疫苗是WHO專家認為相對優秀且有發展潛力的疫苗,是非常好的一件事;第二個意義是由WHO贊助臨床試驗相關費用,對於台灣國產疫苗而言,是非常不容易;第三個意義是在各國專家監督下,若高端疫苗臨床試驗通過後,相信有助於未來高端疫苗取得WHO認可疫苗的機會將增大。目前高端疫苗也獲准於巴拉圭執行新冠肺炎疫苗第三期臨床試驗。
為了防疫,各國也加強入境管制措施,目前僅帛琉、紐西蘭與印尼承認高端疫苗,部分國家有限度放寬檢疫措施,民眾出國前還是要先查明相關規定。自11月8日起,入境美國需要完成兩劑疫苗接種與3日陰性檢驗報告,目前美國承認的疫苗品牌有:莫德納(Moderna)、輝瑞/BNT、嬌生(Johnson & Johnson)、AZ(AstraZeneca)、印度版AZ疫苗Covishield、中國國藥以及中國科興疫苗;歐盟則是承認莫德納、輝瑞/BNT、嬌生以及AZ,凡接種過四種經歐盟認證的疫苗,持有篩檢陰性證明,或染疫後的康復者,都可以將資料輸入數位疫苗護照,並能自由進出歐盟各國,如果高端成功取得國際認證,對台灣民眾來說是一大利多。
第12輪公費疫苗接種在10月22日到27日進行,這次的接種規模有超過百萬人有資格登記,首次全年齡開放,經過一周的施打後,我國第一劑的新冠疫苗的覆蓋了也突破七成大關。
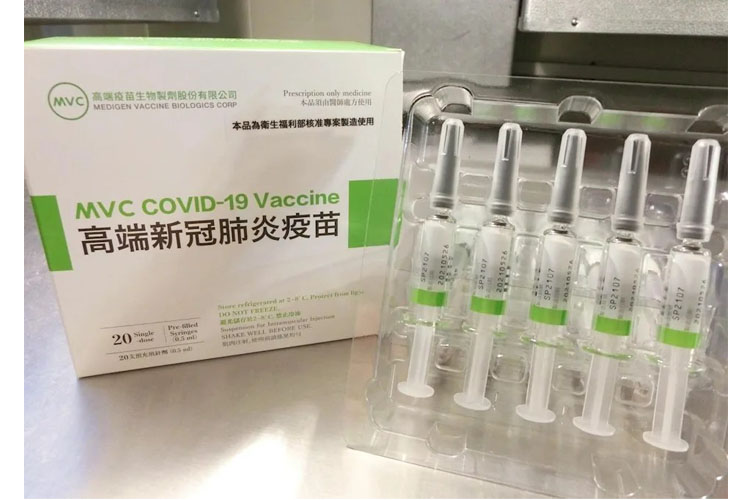
↑世界衛生組織在10月26日宣布,啟動「團體試驗疫苗」計畫,台灣國產高端疫苗被列為候選疫苗。